上海科研团队合作首创体内高通量功能获得性扰动测序平台,“功能图谱+数据库”实现高效精准靶点筛选 2026-04-24 来源:市科委
将近千个转录因子通过病毒载体一次性地精准运送到小鼠脑部的星形胶质细胞,然后对近40万个星形胶质细胞进行蛋白质功能获得性表型高通量分析,由此绘制出星形胶质细胞转录因子功能图谱。这是由中国科学院脑科学与智能技术卓越创新中心周海波研究组与上海市第六人民医院郑元义教授团队、上海鲸奇生物胡新德研究团队合作研究开发的全球首个体内功能获得性扰动测序平台——iGOF-Perturb-seq,所展示的强大能力。
随后,研究团队按图索骥,开创性地在模拟疾病的条件下筛选出一批与阿尔茨海默病相关的转录因子,而其中一个转录因子在患病小鼠模型上展现出显著的治疗效果。
该成果建立了一个位于体内的高通量基因功能研究与靶点筛选平台,建立了针对各种神经系统疾病靶点的预测数据库,不仅为揭示体内基因调控网络与疾病发生机制提供了重要数据支撑,也为后续筛选针对多种脑部疾病的潜在治疗靶点奠定了关键基础。相关论文4月24日在国际学术期刊《科学》在线发表。
实现体内高通量扰动测序
基因是细胞功能的最核心调控者,知道每一个基因在正常与生病状态下的运行情况,对于研究生命运行过程和治疗疾病有着重要的意义。然而,仅仅是一个小鼠细胞中就有2万到3万个蛋白编码基因,要想在体内一个个研究几乎是一件“不可能完成的任务”。
于是,科学家们将目光投向了调控基因转录的关键蛋白——转录因子,并开发了功能获得性扰动测序平台。在小鼠体内,转录因子数量为1000-2000个。“该技术可以高通量解析基因发生变化时是如何影响到转录组的,进而预测对于细胞功能的影响。”周海波说,此前,扰动测序技术主要集中应用于体外体系,不能很好地反映体内真实的生理和病理情况,而对于体内的研究,往往局限于小规模的功能缺失效应,尚缺乏大规模研究功能获得性效应的体内方案。
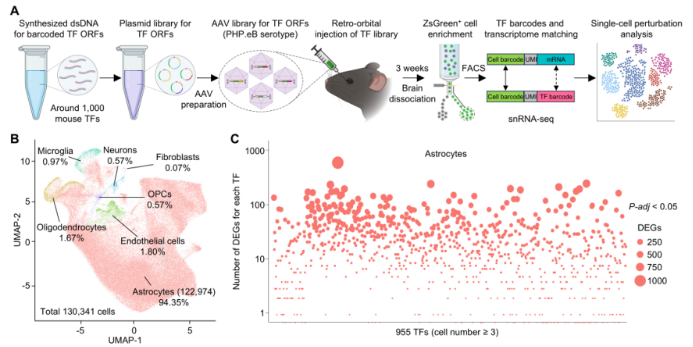
体内高通量功能获得性扰动测序平台的建立
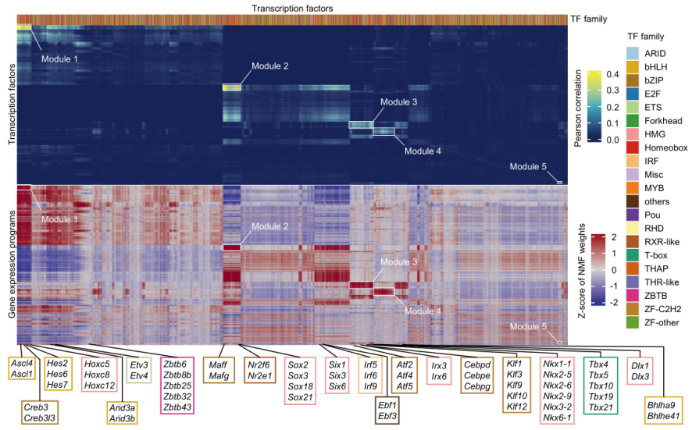
利用此平台产生的扰动细胞转录组信息,研究人员成功绘制了星形胶质细胞转录因子的系统性功能图谱,不仅从分子网络中呈现出转录因子(TF)与靶基因的调控关系,更通过体外细胞模型与在体动物实验,验证了图谱的准确性与可重复性。在此基础上,研究团队进一步构建了转录因子扰动与基因程序响应的体内关联模型,识别出多个具有协同调控作用的TF功能模块,揭示了星形胶质细胞内基因程序的模块化调控特征。同时,借助该模型,团队对此前功能未知或研究较少的转录因子进行了功能注释,明确了它们在调控星形胶质细胞氧化应激和炎症与免疫反应等功能中的潜在作用,为后续机制研究提供了新的线索与依据(图2)。
针对这一空白,周海波团队与郑元义团队、胡新德团队合作,开发了iGOF-Perturb-seq体内高通量功能获得性扰动测序平台。该平台通过整合条形码化开放阅读框、腺相关病毒介导的基因递送以及单细胞核RNA测序技术,实现了在活体组织中对基因功能获得性效应的大规模系统性研究。
锚定星形胶质细胞
在我们的神经系统中,星形胶质细胞与神经元细胞一样广泛分布。它们发挥着极为重要的功能,比如为神经元细胞提供营养支持、调节血流、参与突触发生与成熟、吞噬脑部产生的废物等。
星形胶质细胞对外界刺激非常敏感,一旦中枢神经系统因为疾病、感染或损伤时,它们就会发生形态、分子、功能的变化,乃至蜕化为毒性状态。“毒性星形胶质细胞不仅不能够‘供养’神经元细胞,还会释放很多毒素,破坏神经细胞。”周海波介绍说,“在不少神经退行性疾病,如阿尔茨海默病、帕金森病、亨廷顿病、渐冻症,甚至中风病人体内都存在大量毒性状态星形胶质细胞。”
大脑星形胶质细胞中转录因子的功能注释
近年来,越来越多研究发现,在动物模型中,调控星形胶质细胞反应性状态,避免其走向“异常化”“毒化”,可以有效干预那些依然缺乏有效治疗手段的神经退行性疾病。此外,更加难以治疗的精神类疾病,如抑郁症、精神分裂症、双相情感障碍等,也与星形胶质细胞紧密相关。周海波说,如果能够全面了解星形胶质细胞功能,或将为治疗神经退行性疾病和精神类疾病提供一批全新的靶点。而这也是研究团队坚定地将iGOF-Perturb-seq首先应用于星形胶质细胞的原因。
首张图谱助力靶点高效筛选
研究团队把腺相关病毒(AAV)载体当作“智能快递员”,将近1000个转录因子一次性“整合打包”,精确递送到小鼠的星形胶质细胞里。每个“包裹”都自带一个独特的“身份证”条形码。利用单细胞测序技术,研究人员读取了近40万个星形胶质细胞的转录组“工作日志”,通过条形码把每个细胞的状态和它收到的“包裹”一一对应起来,由此获得了海量的扰动细胞转录组信息。
从这些繁杂的信息中,研究人员成功绘制了首张“星形胶质细胞转录因子的系统性功能图谱”,构建了转录因子扰动与基因程序响应的体内关联模型,不仅准确呈现出转录因子与靶基因的调控关系,还别出多个具有协同调控作用的转录因子功能模块。同时,团队对此前功能未知或研究较少的转录因子进行了功能注释,明确了它们在调控星形胶质细胞功能中的潜在作用。
当研究人员将图谱与来自多种神经退行性疾病、正常衰老、胶质瘤及精神疾病患者的数据集进行关联后,预测了不同脑部疾病相关的候选转录因子。他们共筛选出了39个候选分子,并模仿神经炎症进行测试,结果发现了一个最出色的“修复师”——转录因子Ferd3l。
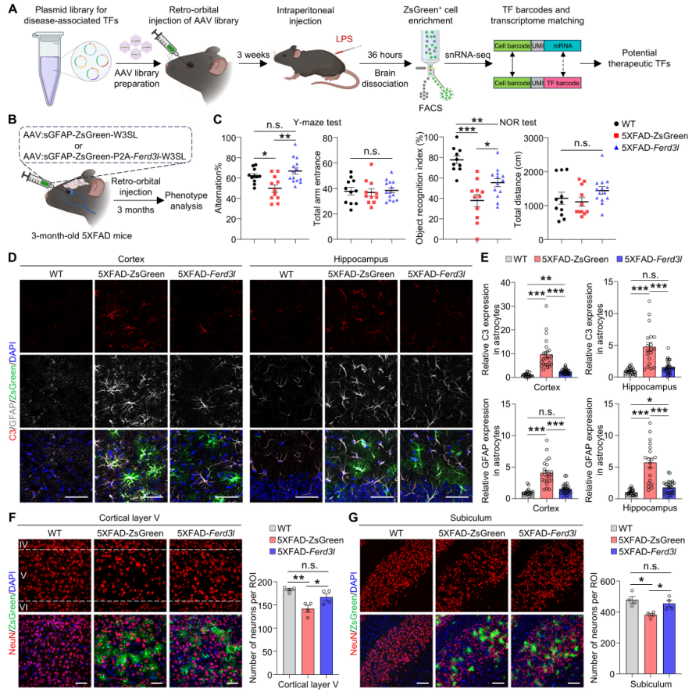
疾病治疗型转录因子的筛选和体内功能验证
为了检验Ferd3l的真实效果,研究人员在模拟人类阿尔茨海默病的小鼠身上进行了测试。结果令人振奋:通过静脉注射进入患病小鼠的Ferd3l,遍布整个大脑星形胶质细胞,让小鼠的认知障碍得到显著改善。这些小鼠在新物体识别和Y迷宫测试中,表现得接近健康小鼠。Ferd3l不仅让星形胶质细胞本身变得“温和”,还重建了它们与神经元、小胶质细胞等其他脑细胞之间“健康”联系,让原本混乱、充满攻击性的脑内环境,恢复成有序、协作的网络。
“基于新平台,我们可以很快把研究与筛选体系扩展到其他细胞中。”周海波坦言,“只需要把星形胶质细胞的启动子换成神经元启动子,就可以构建神经元的扰动数据库,并有望从中发现大量疾病治疗靶点,因为几乎每一种神经疾病都与神经元相关。我们已经开展相关研究了。”